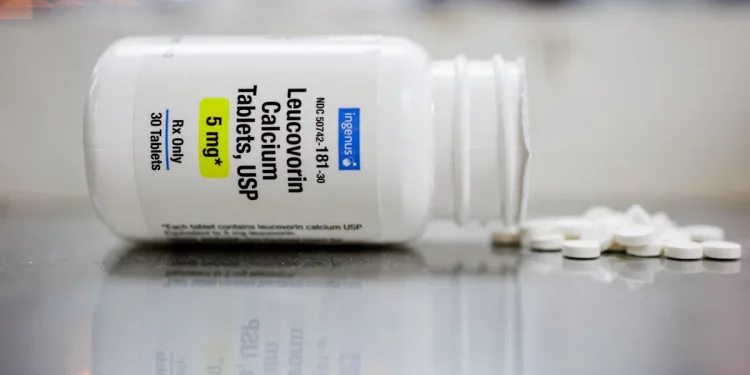
사진/ 더가디언(Leucovorin. Photograph: Hannah Beier/Reuters)
미 식품의약국(FDA)이 수십 년간 사용돼 온 처방용 비타민 제제 루코보린(leucovorin)을 희귀 유전질환 치료제로 처음 승인했다. 이번 결정은 최근 미국 정부가 이 약물을 자폐 스펙트럼 증상 치료 가능성으로 언급하면서 의료계 논쟁이 이어진 가운데 내려졌다.
FDA는 10일(화) 루코보린을 대뇌 엽산 결핍증(cerebral folate deficiency) 치료제로 승인했다고 밝혔다. 이 질환은 체내 필수 비타민인 엽산이 뇌로 제대로 전달되지 못하는 희귀 유전질환으로 영유아기에 발병해 발달 지연, 경련, 근육 조절 장애 등 심각한 신경학적 증상을 일으킬 수 있다.
루코보린은 비타민 B9의 합성 형태인 폴리닉산(folinic acid)으로 지금까지는 항암 치료 과정에서 발생하는 독성 부작용을 완화하는 약물로 널리 사용돼 왔다. FDA 관계자들은 이번 승인 과정에서 처음에는 루코보린의 자폐 스펙트럼 장애(ASD) 치료 가능성에 대한 광범위한 검토를 진행했지만, 과학적 근거가 충분하지 않다고 판단해 적용 대상을 대뇌 엽산 결핍증 환자로 좁혔다고 설명했다.
FDA 관계자는 언론 브리핑에서 “현재 데이터만으로는 자폐 환자 전체에 대한 치료 효과를 입증했다고 말하기 어렵다”며 “다만 관련 기업들이 자폐 환자 대상 임상 연구를 진행하는 데는 열려 있다”고 말했다.
일부 소규모 임상시험에서는 루코보린이 자폐 아동의 언어 능력과 사회적 상호작용 개선에 도움을 줄 수 있다는 결과가 보고된 바 있다. 실제로 일부 부모들은 이 약물을 사용한 뒤 언어 능력이 제한적이던 아이들이 의사소통 능력을 보였다고 주장하기도 했다. 그러나 의료계에서는 해당 연구가 규모가 작고 무작위 대조 임상시험이 부족하다며 신중한 접근이 필요하다는 의견이 지배적이다.
FDA는 이번 승인을 위해 관련 연구 논문과 환자 사례 보고 등을 종합 분석한 체계적 문헌 검토를 근거로 삼았다. 비록 대규모 무작위 임상시험은 없었지만 치료 효과가 비교적 뚜렷하게 나타났다는 점이 승인 판단에 영향을 미쳤다고 FDA 측은 설명했다.
이번 승인으로 루코보린의 제네릭 의약품과 글락소스미스클라인(GSK)의 기존 브랜드 약 ‘웰코보린(Wellcovorin)’에도 같은 적응증이 적용된다.
FDA는 수요 증가에 대비해 기존 제조사들에게 생산 확대도 요청했다. 다만 GSK는 1983년부터 1997년까지 해당 약을 판매했지만 현재로서는 제품 재출시 계획이 없다고 밝힌 상태다.
트레이시 베스 호그 FDA 의약품평가연구센터(CDER) 대행 국장은 성명에서 “이번 승인은 초희귀 질환 환자에게 효과적인 치료법을 신속히 찾으려는 FDA의 노력과 동시에 동일한 과학적 근거 기준을 유지하려는 원칙을 보여주는 사례”라고 말했다.
안미향 기자 amiangs0210@gmail.com














![[영상] 중앙선관위 재외선거 신고신청 유튜브 제작 배포](https://texasn.com/wp-content/uploads/2025/04/Screenshot-2025-04-11-at-10.23.08 AM-120x86.png)




![[단독] 텍사스 ‘K-경제 벨트’ – 실리콘밸리 강화… 산타클라라 상공회의소, 오스틴과 휴스턴 각각 업무협약](https://texasn.com/wp-content/uploads/2026/04/4H2A3738-2-120x86.jpg)

